Autors:
Frank Hunt
Radīšanas Datums:
13 Martā 2021
Atjaunināšanas Datums:
1 Jūlijs 2024

Saturs
- Lai soli
- 1. metode no 3: pH mērītāja izmantošana
- 2. metode no 3: ar lakmusa papīru
- 3. metode no 3: pH izpratne
Ir svarīgi izmērīt ūdens pH līmeni - skābuma pakāpi vai sārmainību. Ūdeni izmanto augi un dzīvnieki, no kuriem mēs esam atkarīgi, un mēs to dzeram katru dienu. Ūdens pH vērtība var liecināt par iespējamo piesārņojumu, tāpēc ūdens pH mērīšana var būt svarīgs sabiedrības veselības aizsardzības pasākums.
Lai soli
1. metode no 3: pH mērītāja izmantošana
 Kalibrējiet zondi un skaitītāju saskaņā ar rūpnīcas instrukcijām. Jums var būt nepieciešams kalibrēt skaitītāju, izmantojot vielu ar zināmu pH vērtību. Skaitītāju var noregulēt atbilstoši šai vielai. Ja gatavojaties testēt ūdeni ārpus laboratorijas, ieteicams veikt šo kalibrēšanu dažas stundas pirms lauka pārbaudes.
Kalibrējiet zondi un skaitītāju saskaņā ar rūpnīcas instrukcijām. Jums var būt nepieciešams kalibrēt skaitītāju, izmantojot vielu ar zināmu pH vērtību. Skaitītāju var noregulēt atbilstoši šai vielai. Ja gatavojaties testēt ūdeni ārpus laboratorijas, ieteicams veikt šo kalibrēšanu dažas stundas pirms lauka pārbaudes. - Pirms lietošanas zondi noskalojiet ar tīru ūdeni. Nosusiniet ar tīru drānu.
 Paņemiet ūdens paraugu un ielejiet to tīrā traukā.
Paņemiet ūdens paraugu un ielejiet to tīrā traukā.- Ūdenim jābūt pietiekami dziļam, lai iegremdētu elektroda galu.
- Atstāj paraugu uz laiku, lai temperatūra stabilizētos.
- Izmēra parauga temperatūru ar termometru.
 Noregulējiet skaitītāju atbilstoši parauga temperatūrai. Zondes jutību ietekmē ūdens temperatūra, tāpēc mērījumi var būt precīzi tikai tad, ja ievadāt temperatūras datus.
Noregulējiet skaitītāju atbilstoši parauga temperatūrai. Zondes jutību ietekmē ūdens temperatūra, tāpēc mērījumi var būt precīzi tikai tad, ja ievadāt temperatūras datus.  Novietojiet zondi paraugā. Pagaidiet, līdz skaitītājs sasniedz līdzsvaru. Skaitītājs ir vienmērīgā stāvoklī, kad rādījums ir stabils.
Novietojiet zondi paraugā. Pagaidiet, līdz skaitītājs sasniedz līdzsvaru. Skaitītājs ir vienmērīgā stāvoklī, kad rādījums ir stabils.  Izlasiet parauga pH mērījumu. PH mērītājs dod rezultātu skalā no 0 līdz 14. Ja ūdens ir tīrs, vērtība ir aptuveni 7. Pierakstiet savus secinājumus.
Izlasiet parauga pH mērījumu. PH mērītājs dod rezultātu skalā no 0 līdz 14. Ja ūdens ir tīrs, vērtība ir aptuveni 7. Pierakstiet savus secinājumus.
2. metode no 3: ar lakmusa papīru
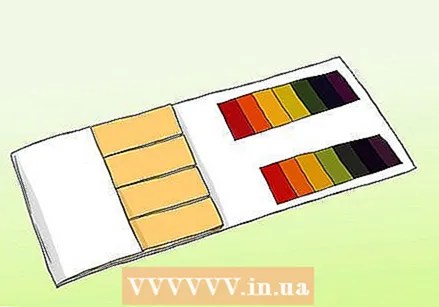 Uzziniet atšķirību starp pH papīru un lakmusa papīru. Lai iegūtu precīzu parauga nolasījumu, varat izmantot pH papīru. Tomēr pH papīru nedrīkst jaukt ar parasto lakmusa papīru. Abus var izmantot, lai pārbaudītu skābes un bāzes, taču tie atšķiras svarīgos aspektos.
Uzziniet atšķirību starp pH papīru un lakmusa papīru. Lai iegūtu precīzu parauga nolasījumu, varat izmantot pH papīru. Tomēr pH papīru nedrīkst jaukt ar parasto lakmusa papīru. Abus var izmantot, lai pārbaudītu skābes un bāzes, taču tie atšķiras svarīgos aspektos. - pH sloksnēs ir virkne indikatoru joslu, kas, pakļaujoties šķīdumam, maina krāsu. Katrā stienī esošo skābju un bāzu stiprums atšķiras. Pēc izmaiņām krāsu modeli var salīdzināt ar paraugiem, kas piegādāti komplektā.
- Lakmusa papīrs ir papīra sloksne, kas satur skābi vai bāzi (sārmainu). Visizplatītākās svītras ir sarkanas (ar skābi, kas reaģē ar bāzēm) un zilas (ar bāzi, kas reaģē ar skābēm). Sarkanās svītras kļūst zilas, ja viela ir sārmaina, un zilās svītras kļūst sarkanas, ja viela ir skāba. Lakmusa papīrus var izmantot kā ātru un vienkāršu testu, taču lētākās šķirnes ne vienmēr precīzi mēra šķīduma stiprumu.
 Paņemiet ūdens paraugu un ielejiet to tīrā traukā. Ūdenim jābūt pietiekami dziļam, lai sloksni iegremdētu.
Paņemiet ūdens paraugu un ielejiet to tīrā traukā. Ūdenim jābūt pietiekami dziļam, lai sloksni iegremdētu.  Iemērciet testa sloksni paraugā. Pietiek ar dažu sekunžu ekspozīciju. Indikatora joslas uz papīra pēc dažiem mirkļiem mainīs krāsu.
Iemērciet testa sloksni paraugā. Pietiek ar dažu sekunžu ekspozīciju. Indikatora joslas uz papīra pēc dažiem mirkļiem mainīs krāsu.  Salīdziniet testa sloksnes galu ar krāsu diagrammu, kas pievienota papīram. Kartītes krāsai vai krāsām jāatbilst krāsai vai krāsām uz testa sloksnes. Pēc tam krāsu karte krāsu modeļus saista ar pH līmeni.
Salīdziniet testa sloksnes galu ar krāsu diagrammu, kas pievienota papīram. Kartītes krāsai vai krāsām jāatbilst krāsai vai krāsām uz testa sloksnes. Pēc tam krāsu karte krāsu modeļus saista ar pH līmeni.
3. metode no 3: pH izpratne
 Uzziniet, kā tiek noteiktas skābes un bāzes. Skābumu un sārmainību (termins, ko lieto, lai aprakstītu bāzes) gan nosaka ūdeņraža joni, ko tie ziedo vai uzņem. Skābe ir viela, kas ziedo (vai "ziedo") ūdeņraža jonus, un bāze ir viela, kas absorbē papildu ūdeņraža jonus.
Uzziniet, kā tiek noteiktas skābes un bāzes. Skābumu un sārmainību (termins, ko lieto, lai aprakstītu bāzes) gan nosaka ūdeņraža joni, ko tie ziedo vai uzņem. Skābe ir viela, kas ziedo (vai "ziedo") ūdeņraža jonus, un bāze ir viela, kas absorbē papildu ūdeņraža jonus.  Izprotiet pH skalu. PH skaitli izmanto ūdenī šķīstošo vielu skābuma vai sārmainības pakāpes mērīšanai. Ūdenī parasti ir vienāds daudzums hidroksīda jonu (OH−) un hidronija jonu (H3O +). Hidroksīda un hidronija jonu attiecība mainās, ja ūdenim pievieno skābu vai sārmainu vielu.
Izprotiet pH skalu. PH skaitli izmanto ūdenī šķīstošo vielu skābuma vai sārmainības pakāpes mērīšanai. Ūdenī parasti ir vienāds daudzums hidroksīda jonu (OH−) un hidronija jonu (H3O +). Hidroksīda un hidronija jonu attiecība mainās, ja ūdenim pievieno skābu vai sārmainu vielu. - Parasti to uzskata par skalu, kas svārstās no 0 līdz 14 (lai gan vielas var arī neiekļauties šajā diapazonā). Neitrālu vielu vērtējums ir aptuveni 7, skābās vielas ir zem 7 un sārmainās - virs 7.
- PH skala ir logaritmiska, tas nozīmē, ka veselu skaitļu atšķirības norāda desmitkārtīgu skābuma vai sārmainības atšķirību. Piemēram, viela ar pH 2 ir desmit reizes skābāka nekā viela ar pH 3 un 100 reizes skābāka nekā viela ar pH 4. Skala darbojas tāpat kā ar sārmainām vielām, ar jebkuru citu vesels skaitlis ir desmitkārtīga starpība.
 Uzziniet, kāpēc mēs pārbaudām ūdens pH. Tīrā ūdens pH ir 7, bet holandiešu krāna ūdens pH parasti ir no 7,5 līdz 8,3. Ļoti skābs ūdens (ūdens ar zemu pH vērtību), visticamāk, izšķīdina toksiskas ķīmiskas vielas. Tie var piesārņot ūdeni un padarīt to nedrošu dzert.
Uzziniet, kāpēc mēs pārbaudām ūdens pH. Tīrā ūdens pH ir 7, bet holandiešu krāna ūdens pH parasti ir no 7,5 līdz 8,3. Ļoti skābs ūdens (ūdens ar zemu pH vērtību), visticamāk, izšķīdina toksiskas ķīmiskas vielas. Tie var piesārņot ūdeni un padarīt to nedrošu dzert. - Parasti ieteicams pārbaudīt pH uz vietas. Ja laboratorijas pētījumiem ņemat ūdens paraugu, oglekļa dioksīds (CO2) no gaisa var izšķīst ūdenī. Izšķīdušais oglekļa dioksīds reaģē ar ūdenī esošajiem joniem un palielina skābumu bāziskos vai neitrālos šķīdumos. Lai izvairītos no oglekļa dioksīda piesārņošanas, ūdens jāpārbauda divu stundu laikā pēc savākšanas.