Autors:
Randy Alexander
Radīšanas Datums:
2 Aprīlis 2021
Atjaunināšanas Datums:
1 Jūlijs 2024

Saturs
Ķīmiskais vienādojums ir ķīmiskās reakcijas simbolisks attēlojums. Reaģenti ir rakstīti kreisajā pusē, bet produkts - labajā pusē. Masas saglabāšanas likums norāda, ka ķīmiskās reakcijas laikā neviens atoms nedzimst un nezaudē, tāpēc reaktantā esošo atomu skaitam jābūt vienādam ar reakcijā esošo atomu skaitu. produktu. Pēc šīs apmācības jūs varat līdzsvarot ķīmiskos vienādojumus dažādos veidos.
Soļi
1. metode no 2: bilance pēc tradicionālās metodes
Uzrakstiet doto vienādojumu. Šajā piemērā jums būtu: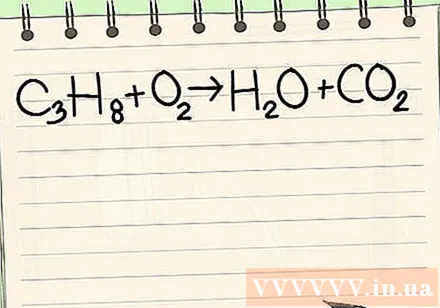
- C3H8 + O2 -> H2O + CO2
- Šī reakcija notiek propāna (C3H8sadedzina skābeklī, veidojot ūdeni un oglekļa dioksīdu.

Pierakstiet katra elementa atomu skaitu katrā vienādojuma pusē. Skatiet indeksus zem katra atoma, lai atrastu atomu skaitu vienādojumā.- Pa kreisi: 3 ogleklis, 8 ūdeņradis un 2 skābeklis.
- Pa labi: 1 ogleklis, 2 ūdeņradis un 3 skābeklis.
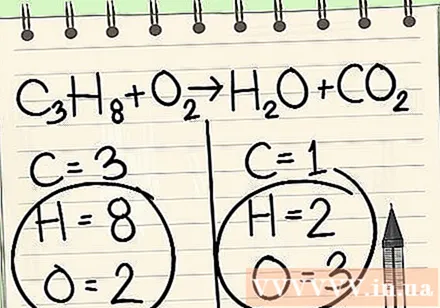
Galu galā vienmēr atstājiet ūdeņradi un skābekli.
Ja līdzsvarošanai ir atlicis vairāk nekā viens elements: Atlasiet elementu, kas parādās tikai atsevišķā reaģenta molekulā un tikai produkta atsevišķā molekulā. Tas nozīmē, ka vispirms jums būs jāsabalansē oglekļa atomi.
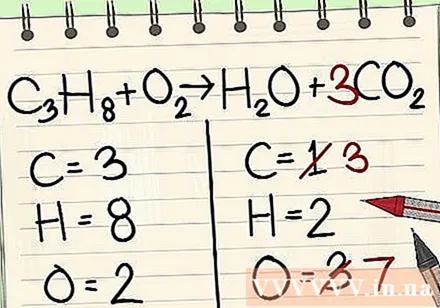
Pievienojiet vienotu oglekļa atomu koeficientu vienādojuma labajā pusē, lai līdzsvarotu to ar trim oglekļa atomiem vienādojuma kreisajā pusē.- C3H8 + O2 -> H2O + 3CO2
- Faktors 3 oglekļa priekšā labajā pusē norāda, ka ir 3 oglekļa atomi, jo kreisajā pusē esošais apakšgrupa 3 norāda uz 3 oglekļa atomiem.
- Ķīmiskajā vienādojumā jūs varat mainīt koeficientu, bet ne indeksu.
Nākamais ir ūdeņraža atomu līdzsvars. Jums kreisajā pusē ir 8 ūdeņraža atomi. Tādējādi jums vajadzēs 8 labajā pusē.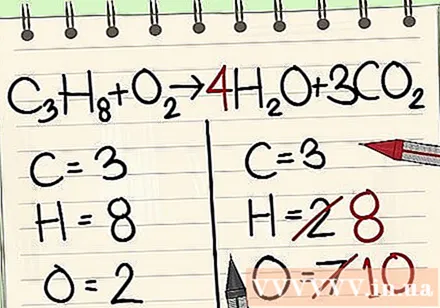
- C3H8 + O2 -> 4H2O + 3CO2
- Stundas labajā pusē kā koeficientu pievienojat 4, jo apakšējais skaitlis parāda, ka jums jau ir 2 ūdeņraža atomi.
- Reizinot koeficientu 4 ar indeksu 2, iegūsiet 8.
- Pārējie 6 skābekļa atomi ir no 3CO2. (3x2 = 6 skābekļa atomi + 4 citi skābekļa atomi = 10)
Līdzsvaro skābekļa atomus.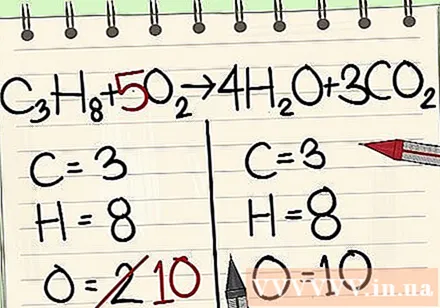
- Tā kā jūs esat pievienojis koeficientus molekulām pa labi no vienādojuma, skābekļa atomu skaits ir mainījies. Tagad jums ir 4 skābekļa atomi ūdens molekulā un 6 skābekļa atomi oglekļa dioksīda molekulā. Kopumā mums ir 10 skābekļa atomi.
- Pievienojiet koeficientu 5 skābekļa molekulai pa kreisi no vienādojuma. Tagad jums ir 10 skābekļa molekulas katrā pusē.
- C3H8 + 5O2 -> 4H2O + 3CO2.

- Oglekļa, ūdeņraža un skābekļa atomi ir līdzsvarā. Jūsu vienādojums ir pabeigts.
2. metode no 2: Bilance saskaņā ar algebrisko metodi
Uzrakstiet vienādojumus pēc simboliem un formulām. Piemērs a = 1 un uzrakstiet vienādojumu, pamatojoties uz šo formulu.
Ciparus aizstājiet ar to mainīgajiem.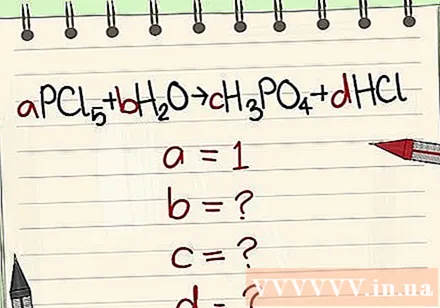
Pārbaudiet elementu daudzumu reakcijas pusē, kā arī produkta pusi.
- Piemērs: aPCl5 + bH2O = cH3PO4 + dHCl tā, ka a = 1 b = c = d = un atdalot elementus P, Cl, H, O, tādējādi iegūstot a = 1 b = 4 c = 1 d = 5 .
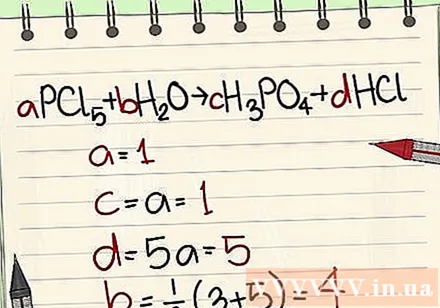
- Piemērs: aPCl5 + bH2O = cH3PO4 + dHCl tā, ka a = 1 b = c = d = un atdalot elementus P, Cl, H, O, tādējādi iegūstot a = 1 b = 4 c = 1 d = 5 .
Padoms
- Atcerieties vienkāršot vienādojumu.
- Ja jums ir problēmas, tiešsaistes bilances rīkā varat ierakstīt vienādojumu, lai to līdzsvarotu. Atcerieties, ka, kārtojot eksāmenu, jums nav piekļuves tiešsaistes bilancei, tāpēc neesiet no tā atkarīgs.
Brīdinājums
- Ķīmiskajā vienādojumā nekad neizmantojiet koeficientu kā daļu - jūs nevarat sadalīt molekulas vai atomus ķīmiskajā reakcijā.
- Līdzsvara procesa laikā jūs varat izmantot frakcijas, taču vienādojums netiks līdzsvarots, ja koeficienti joprojām ir frakcijas.
- Lai noņemtu frakcijas, reiziniet visu vienādojumu (gan pa kreisi, gan pa labi) ar frakcijas saucēju.